Открытие нейтрона и возникновение нейтронно-протонной теории строения ядра
Ядро построено
1932 год оказался на удивление богатым историческими событиями в ядерном мире.
Один из учеников Резерфорда, Джеймс Чадвик, направил поток альфа-частиц на пластинку бериллия, за которой была установлена камера Вильсона. Из бериллия в результате бомбардировки вылетали какие-то новые тяжелые частицы. Их столкновение с ядрами аргона или азота в камере Вильсона привело к превращениям, приоткрывшим наконец завесу над тайной строения самих ядер.
Новые частицы не только обладали тяжелой массой — они были совершенно нейтральны и отличались большой проникающей способностью. Свободно проходя через достаточно толстые слои газа, эти частицы не вызывали его ионизации, не «отрывали» электроны от атомов. Верный признак, достаточно точно отличающий нейтральную частицу от заряженной…
Новую частицу назвали нейтроном. Ее масса оказалась почти такой же, как у протона,— 1838,6 электронной массы. Открытый нейтрон тут же был использован в лабораториях всего мира для «изготовления» ядерных снарядов. Ими немедленно начали облучать ядра азота, которые в ответ неожиданно распались на ядра бора и гелия!
Нильс Бор прислал из Копенгагена поздравительное письмо английским коллегам, а Резерфорд ответил: «Мне было приятно услышать, что Вы отнеслись к Нейтрону так благожелательно».
Вы обратили внимание: Нейтрон торжественно написан с большой буквы?
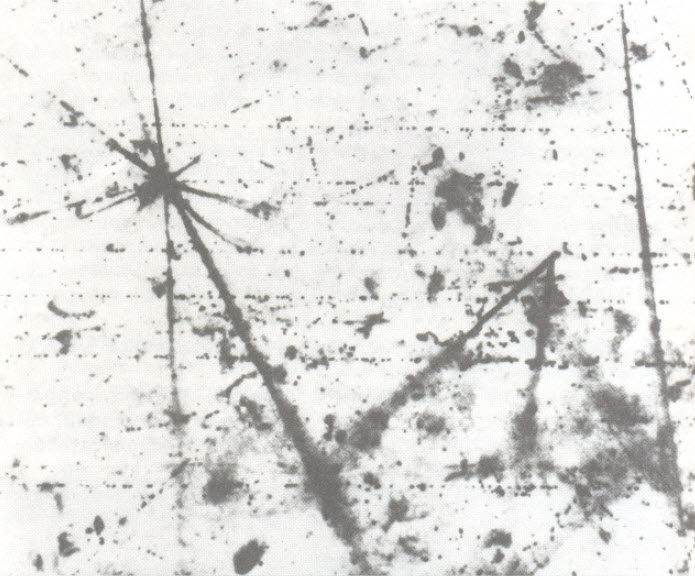
Звезда на этой фотографии, полученной в камере Вильсона, означает момент столкновения протона — ядра водорода с ядром другого атома.
Советский физик Д. Д. Иваненко и немецкий ученый В. Гейзенберг, узнав об открытии нейтрона, выдвинули нейтронно-протонную теорию строения ядра. Теория стала вскоре общепринятой, ее подтверждали многие достаточно точные измерения и эксперименты.
Ядро каждого элемента по этой теории состоит из протонов и нейтронов, объединенных могучими силами взаимодействия (каждая такая пара получила наименование нуклона). Число протонов в ядре равно числу электронов, вращающихся вокруг ядра; оно определяет величину положительного заряда ядра атома. В целом атом при обычных условиях электронейтрален. Количество нейтронов в ядре зависит от атомной массы элемента — с помощью нейтронов каждый химический элемент «добирает» свою массу до значения, положенного ему таблицей Менделеева.
Теория Иваненко — Гейзенберга сумела ответить на вопрос, который давно волновал как физиков, так и химиков: почему в природе часто встречаются химические элементы с одним и тем же зарядом ядра и почти одинаковые по свойствам, но вот их атомные массы все же немного отличаются? Объяснение оказалось удивительно простым: эти вещества представляют собой изотопы — едва различимые разные виды одного и того же элемента; многоликость создается оттого, что каждый элемент может содержать в ядре при неизменном и одинаковом числе протонов (ведь от него зависит главное — заряд атомного ядра!) разное число нейтронов.
Дмитрий Иванович Менделеев сначала расположил элементы в ряд, руководствуясь одним правилом — возрастанием атомной массы, и неизвестные в его времена нейтроны внесли некоторую путаницу в знаменитую периодическую таблицу. Вскоре, как мы знаем, во главу угла совершенно справедливо был положен незыблемый заряд атомного ядра элементов, и все стало на свои места.
Источник: Марк Колтун “Мир физики“.


